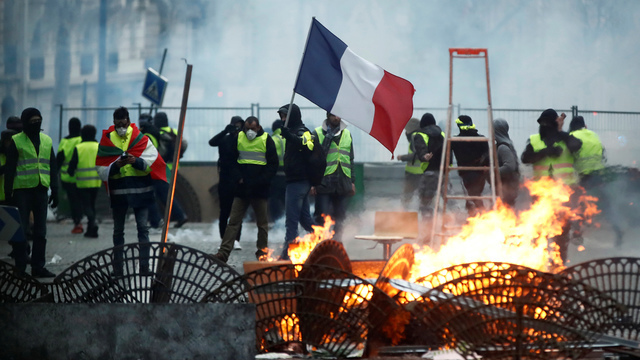Die Produktion von lebensrettenden Schrittmachern für Kinder mit Herzfehlern ist weitgehend eingestellt worden. Das Problem könnte sich weiter verschärfen.
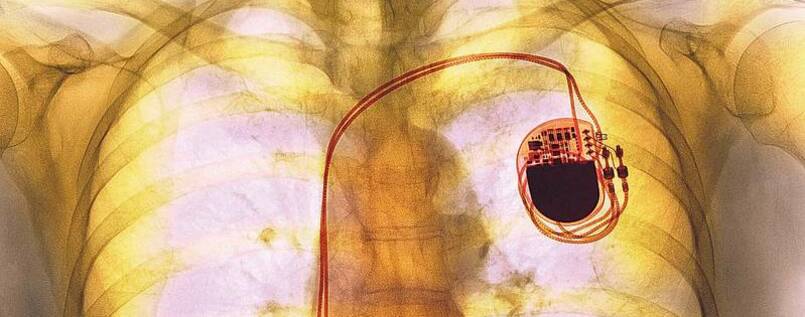 Taktgeber. In der Brust von Erwachsenen finden Herzschrittmacher und Kabel genug Platz. Bei Säuglingen müssen die Ärzte diverse…
Taktgeber. In der Brust von Erwachsenen finden Herzschrittmacher und Kabel genug Platz. Bei Säuglingen müssen die Ärzte diverse…
Jahr für Jahr brauchen rund hundert Kinder mit einem angeborenen Herzfehler einen Herzschrittmacher. Eine überlebensnotwendige Nachfrage, die derzeit nicht gedeckt werden kann. Kürzlich hat ein Neugeborenes aus dem Saarland den letzten kleinen Herzschrittmacher implantiert bekommen, der dort noch verfügbar war (der Tagesspiegel berichtete). Andere spezialisierte Zentren melden inzwischen ebenfalls, dass ihre Vorräte zur Neige gehen. Und das, obwohl es zu „Hamsterkäufen“ gekommen war, als bekannt wurde, dass die Produktion des weltweit kleinsten Schrittmachers eingestellt werden sollte. Auch in den USA sandte die einschlägige Fachgesellschaft PACES (Pediatric and Congenital Electrophysiological Society) einen Hilferuf aus.
Eine Liste des Mangels
In Deutschland hat nun ein Brandbrief mehrerer medizinischer Fachgesellschaften und des Aktionsbündnisses Angeborene Herzfehler, über den der Tagesspiegel berichtete, offenbar die zuständigen deutschen Politik-Ressorts und den Branchenverband der Medizingeräte-Hersteller auf das Problem gestoßen. Nun soll vom Forschungsverbund „Kompetenznetz Angeborene Herzfehler“ eine Liste der kindgerechten Medizinprodukte erstellt werden, die in den Kinderherzzentren fehlen. Darum hatten das Bundesministerium für Gesundheit und der Bundesverband Medizintechnologie anlässlich eines Treffens Mitte Juli gebeten. Zwar wurde das Kompetenznetz schon 2003 mit dem Ziel gegründet, die Versorgung von Menschen mit angeborenem Herzfehler zu verbessern. Engpässe gibt es aber nicht nur bei Herzschrittmachern: Es mangelt auch an kindgerechten Stents, Kathetern oder Zangen für Gewebeentnahmen. „Die Teilnehmer des Treffens haben eingeräumt, dass man die Situation der Kinder bisher nicht bedacht hat“, sagt die Ärztin Ulrike Bauer, Geschäftsführerin des Kompetenznetzes.
Inzwischen hat die US-Firma Abbott, Hersteller des „Microny“-Schrittmachers, den das Neugeborene aus dem Saarland bekam und der derzeit Mangelware ist, zugesichert, man werde die Produktion fortsetzen und zudem in die Entwicklung eines neuen Geräts speziell für Babys investieren, „obwohl es selten gebraucht wird“. Was daraus wird, bleibt abzuwarten.
Standard ist: Ärzte müssen improvisieren
In der Herzmedizin für Kinder sei man gewohnt, mit Kompromissen zu leben, zu improvisieren und Materialien anzuwenden, die eigentlich für Erwachsene hergestellt wurden, sagt der Charité-Kinderkardiologe Felix Berger, Direktor der Klinik für Angeborene Herzfehler am Deutschen Herzzentrum und der Charité und Mitglied im Lenkungsausschuss des Kompetenznetzes. Ein besonders gutes Beispiel für die Improvisationskünste der Mediziner sind die Gefäßstützen: Stents, wie sie millionenfach die kleineren, peripheren Arterien Älterer offen halten, werden bei den Kleinsten für große Gefäße eingesetzt.
Spätestens bei komplizierten mehrteiligen Produkten wie den Schrittmachern stößt die Flexibilität der Mediziner aber an ihre Grenzen. Allein das ein Meter lange Kabel eines Erwachsenen-Schrittmachers im Körper eines Babys unterzubringen ist eine Herausforderung. Hashim Abdul-Khaliq, Direktor der Pädiatrischen Kardiologie am Uniklinikum des Saarlandes und Sprecher des Kompetenznetzes Angeborene Herzfehler, hat beim Treffen im Gesundheitsministerium demonstriert, wie viele Schlaufen er dafür machen muss. „Es trifft uns natürlich, wenn besonders geeignete Produkte nicht mehr hergestellt werden“, sagt auch Charité-Mediziner Felix Berger. Erschwerend kommt hinzu, dass viele derartige technische Hilfen für den wachsenden Organismus nicht auf Dauer geeignet sind, da sie nicht mitwachsen. Die Kinder brauchen folglich im Lauf der Jahre wiederholt Ersatz.
Mitwachsende Zellen statt starrer Apparate
Was Forscher vom Institut für Angewandte Medizintechnik der Technischen Hochschule in Aachen und der Mediziner Stefan Jockenhövel in Zusammenarbeit mit der dortigen Uniklinik für Kinderkardiologie derzeit austüfteln, soll den Heranwachsenden eines Tages wiederholte Eingriffe ersparen: Sie wollen aus körpereigenen Hautzellen durch Reprogrammierung Herzmuskelzellen machen, diese Zellen züchten und zu fadenförmigen biologischen Kabeln verbinden. Nach einem gezielten Stimulationsprogramm sollen die Bio-Kabel ein eigenes Erregungssystem entwickeln und sich ans Blutgefäßsystem anschließen, um die Überleitung der elektrischen Erregung vom Vorhof des Herzens zur Herzkammer zu übernehmen. Kindern mit einer angeborenen Blockade dieser Überleitung („AV-Block“) soll auf diese Weise dauerhaft geholfen werden, da die biologischen Elektrokabel im Idealfall mitwachsen. Der Nachwuchswissenschaftler Hans Keijdener konnte für das Projekt „BioPacer“ den diesjährigen Crowdfunding-Preis der Stiftung Kinderherz entgegennehmen.
Noch ist der Bio-Schrittmacher Zukunftsmusik. Und durch die im letzten Jahr verabschiedete EU-Verordnung zu Medizinprodukten, die in zwei Jahren in Kraft tritt, wird sich das Problem möglicherweise noch verschärfen, so fürchtet man beim Kompetenznetz. Die Hersteller könnten nämlich ausgerechnet von jenen Auflagen abgeschreckt werden, die vom Gesetzgeber als Schutzmaßnahme für die Patienten gedacht sind. So sollen klinische Studien die Sicherheit der Medizinprodukte verbessern. Das könnte aber dazu führen, dass einige Produkte schlicht nicht mehr verfügbar sind. Große Zulassungsstudien, wie sie auch für neue Medikamente gefordert werden, könne man angesichts der kleinen Patientengruppen nämlich allenfalls in internationaler Zusammenarbeit und auch dann nur mit großer Mühe auf die Beine stellen, gibt Berger zu bedenken. „Herz-Studien mit Kindern zu etablieren ist extrem schwierig, denn Zigtausende von Patienten wie beim Herzinfarkt haben wir – zum Glück für die jungen Patienten – nicht.“ Nicht nur die Produkte sind klein, auch der Markt ist es.
EU-Regularien schrecken Firmen ab
Während den Problemen der Pädiater bei der Zulassung von Medikamenten für Kinder inzwischen mit der 2007 in Kraft getretenen EU-Verordnung über Kinderarzneimittel ansatzweise Rechnung getragen werde, werde sich die Situation bei den Medizinprodukten in Zukunft vermutlich weiter verschärfen, beklagt Berger. Es sei praktisch unmöglich, für jedes Einsatzgebiet eines Medizinprodukts eine eigenständige Zulassungsstudie vorzulegen, wie es eine strenge Auslegung der EU-Verordnung für Medizinprodukte erfordern könnte. Bislang ist etwa die Versorgung der Hauptschlagader von Kindern mit speziellen Stents durch eine entsprechende klinische Studie abgesichert. Die Kinderkardiologen setzen dieselben Stützen allerdings auch in der Lungenarterie ein, also „off label“ – ohne dass es dafür eine eigene Zulassungsstudie gegeben hätte. „Wenn wir wüssten, dass eine auf Erfahrung basierende Handhabung einer Zulassung gleichgestellt und akzeptiert würde, wären wir ruhiger“, sagt der Kinderkardiologe.
„Die Firmen werden von der Produktion kindgerechter Medizinprodukte regelrecht abgeschreckt“, urteilt Robert Cesnjevar, Leiter der Kinderherzchirurgie am Uniklinikum in Erlangen. Die Prüfauflagen liefen ins Leere, „weil es an gesetzlich verankerten Anreizen zu Forschung und Entwicklung von Produkten auch für vergleichsweise geringe Patientenzahlen fehlt.“
Daten über Herzkranke als Ressource für Tests und Zulassungsstudien
Praktische Erfahrungen aus der Behandlung von heranwachsenden und erwachsenen Menschen, die mit einem Herzfehler auf die Welt kamen, werden in Deutschland allerdings längst in gebündelter Form für die Forschung nutzbar gemacht: Im „Nationalen Register für angeborene Herzfehler“ werden auf freiwilliger Basis die Daten zur Behandlung herzkranker Heranwachsender gesammelt – und neben den Daten auch Gewebeproben von Operationen und DNS-Proben der Patienten. Als Grundlage für solide Versorgungsforschung sei das Register, das inzwischen die Daten von über 50.000 Kindern, Jugendlichen und Erwachsenen mit einem angeborenen Herzfehler umfasst, weltweit einzigartig, sagt Ulrike Bauer.
Wirkung zeigten die Daten zum Beispiel, als im vergangenen Jahr ein neues Diagnoseverfahren in das Neugeborenen-Screening aufgenommen wurde, die Pulsoxymetrie. Mittels einer winzigen Manschette wird dafür die Haut am Zeh des Babys durchleuchtet, um zu sehen, wie viel Sauerstoff sein Blut enthält. So lassen sich eine Reihe schwerer Herzfehler ausschließen – wenn frühzeitig untersucht wird. Eine Studie hatte gezeigt, dass selbst schwerwiegende Fehlbildungen und Funktionsstörungen des Herzens oft erst Wochen nach der Geburt diagnostiziert werden – wenn es den Kindern bereits erkennbar schlecht geht.
Für solche Studien sind die Daten des Registers besonders nützlich, machen es aber auch möglich, gezielt Patienten für Studien auszuwählen, in denen etwa neue, kindgerechte Herzschrittmacher oder Stents getestet werden sollen. Vorausgesetzt, solche Geräte werden überhaupt produziert.
Team Liquid gewinnt auch Blast Series Pro in Los Angeles
Los Angeles (dpa) – Unaufhaltsam hat sich Team Liquid bei der Blast Pro Series in Los Ange…